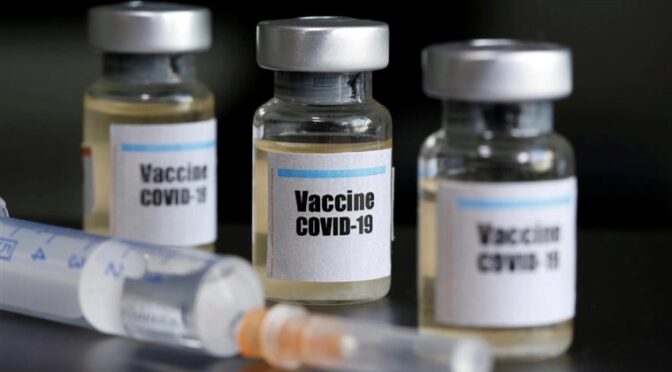
辉瑞公司首席执行官阿尔伯特•博拉( Albert Bourla)今周日表示,如果证明(辉瑞)的COVID-19疫苗安全有效,那么首批疫苗可能会在今年年底前分发给美国人。
博拉在接受哥伦比亚广播公司的“面对全国”节目采访时说,辉瑞将在10月底前获得美国食品和药物管理局(FDA)的后期试验的关键数据。他说,如果FDA批准这种疫苗,该公司将准备分发首批“数十万剂”。
由于新冠大流行,美国卫生官员和制药商一直在通过投资多个阶段的研究来加速开发候选疫苗,尽管如果疫苗最终无效或不安全,这样做可能是徒劳的。
美国制药巨头-辉瑞一直在与德国制药商BioNTech合作。美国政府今年7月宣布,如果证明疫苗安全有效,将向这些公司支付19.5亿美元,用于生产和交付1亿剂疫苗。这项协议是特朗普政府加快研发和生产疫苗和治疗方法以抗击冠状病毒的“扭曲速度行动”的一部分。
博拉同时表示,该公司已经投资15亿美元开发这种潜在的疫苗。他说,如果疫苗失效,这将给公司带来财务上的“痛苦”。
“说到底,只是钱。但这不会让公司破产,尽管这会很痛苦。
辉瑞公司的实验性疫苗含有一种名为Messenger RNA核糖核酸的遗传物质,科学家希望这种物质能激发免疫系统能抗病毒。
辉瑞是目前正在进行疫苗后期测试的三家公司之一。另外两家公司是摩德纳(Moderna)和阿斯利康(AstraZeneca),在出于安全原因暂时暂停试验后,两家公司于周六宣布将恢复试验。
上周六,辉瑞向FDA提交了一份提案,要求将晚期试验扩大到4.4万名参与者,较之前的3万人目标上大幅增加。
据CNBC报道称,在疫苗发展之际,传染病专家和科学家最近几周表示,他们担心美国总统正在向美国食品和药物管理局施压,要在疫苗经过充分测试之前批准疫苗上市。而FDA专员斯蒂芬·哈恩(Stephen Hahn)坚称,他没有受到特朗普的压力要求他们快速研发疫苗,他上个月对英国《金融时报》表示,该机构准备绕过整个联邦审批程序,以便尽快推出Covid-19疫苗。
9月8日,包括辉瑞在内的9家制药公司发布了一封信,承诺在研发冠状病毒疫苗的过程中,他们将优先考虑安全性并维护“科学过程的完整性”。
即使一种疫苗被批准在年底前分发,它也可能供不应求。这种疫苗可能需要以不同的间隔注射两剂,各州仍面临后勤方面的挑战,例如建立分发地点和获得足够的疫苗接种所需的针头、注射器和瓶子。
本月早些时候,美国国家科学院、工程院和医学院发布了一份在美国分发疫苗的建议草案,如果疫苗被批准用于公共用途。这份报告是由美国国立卫生研究院和疾病预防控制中心要求的。
据相关组织称,疫苗将分四个阶段分发,首先让医护人员、老年人和有潜在健康状况的人接种疫苗。基本工人、教师和无家可归者收容所的人以及监狱中的人将是下一个名单,其次是儿童和年轻人。
出门戴口罩,勿去扎人堆!
*重要条例!圣地亚哥县健康与社会服务部,公共卫生服务部发布卫生官命令与应急条例,并于2020年8月22日生效。全文链接在此:
https://www.sandiegocounty.gov/content/dam/sdc/hhsa/programs/phs/Epidemiology/Health_Officer_Order_Chinese.pdf
有关本地COVID-19测试问题咨询和联系的官方网页:
https://www.sandiegocounty.gov/content/sdc/hhsa/programs/phs/community_epidemiology/dc/2019-nCoV/testing.html
加州公共卫生部发布的关于使用布面覆盖物防止新型冠状病毒COVID-19传播的指南链接。https://www.cdph.ca.gov/Programs/CID/DCDC/Pages/Face-Coverings-Guidance.aspx
查查您住的附近有没有COVID-19病例 By 输入你的Zip Code!https://www.coronainusa.com/>
全美校园新型肺炎疫情实时动态
https://www.wholeren.com/coronavirus-update/#/
(美国华文网 圣地亚哥华文网编发 USChinesePress.com SanDiegoChinesePress.com)